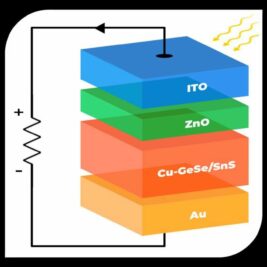
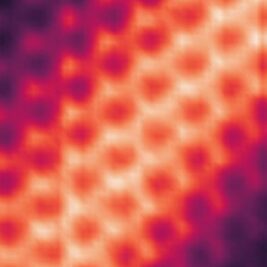
Une équipe internationale de chercheurs, dirigée par l’Université de Göttingen, a démontré expérimentalement que les électrons dans le graphène bicouche naturel se...
Tenez vous au courant de l’actualité énergétique & environnementale…
Vous êtes un nouveau lecteur sur Enerzine.com ? inscrivez-vous à la lettre d’information bi-hebdomadaire. 📰 Vous êtes une entreprise et 🚀 vous voulez faire connaître un service ou un produit auprès de notre lectorat ?
Les dernières actualités

Un convertisseur DC-DC atteint une efficacité record de 98,3%
Les chercheurs de l’Université de Kobe et de l’Université nationale Chung Hsing ont développé un nouveau...
Consulter
Des fibres avec une conductivité électrique 1,3 fois supérieure
Les dispositifs portables, comme les montres connectées et les lunettes de réalité augmentée, sont en train de bousculer le...
Consulter
Des chercheurs repoussent les limites des condensateurs
Les condensateurs électrostatiques, composants essentiels de l’électronique moderne, sont au cœur d’une étude...
Consulter
Réseau quantique : les chercheurs franchissent une étape décisive
La communication quantique à longue distance est un défi majeur pour le développement de réseaux quantiques destinés au calcul...
ConsulterCréer une île paradisiaque dans un réacteur de fusion
La fusion nucléaire, source d’énergie propre et inépuisable, suscite un intérêt croissant dans la communauté scientifique. Les chercheurs du Princeton Plasma...
23 millisecondes : le temps record de mémoire atteint par le tambour...
Les chercheurs de l’Institut Niels Bohr de l’Université de Copenhague ont développé une nouvelle méthode pour créer une mémoire quantique. Un petit tambour...
Les technologies clés de l’intelligence énergétique dans les...
L’avènement de l’intelligence énergétique représente une révolution dans la façon dont les bâtiments et les industries utilisent et gèrent cette ressource...
Un centre high-tech pour relever les défis énergétiques de demain
Le Centre pour la chimie de l’énergie et de l’environnement de Iéna (CEEC Iéna) de l’Université de Iéna (Allemagne) suscite de grandes attentes avant...
La SCIA, moteur de l’innovation dans les semi-conducteurs aux USA
Le carbure de silicium (SiC), un matériau semi-conducteur composé d’atomes de silicium et de carbone arrangés en cristaux, est de plus en plus essentiel aux...
Découverte d’une méthode pour un graphène nanocellulaire parfait
Le graphène, matériau aux propriétés exceptionnelles, ne cesse de susciter l’intérêt de la communauté scientifique depuis sa découverte en 2004. Ses applications...
Comprendre la gestion technique du bâtiment et son utilité
Dans un contexte de réchauffement climatique et de hausse du coût de l’énergie, la mise en place d’un système de gestion technique du bâtiment devient incontournable...
L’hydrogène naturel, une énergie illimitée cachée sous nos pieds ?
L’hydrogène naturel, présent dans les poches souterraines de la croûte terrestre, suscite un intérêt grandissant en tant que source d’énergie potentiellement...
Un filtre intelligent de 10 000 pixels pour un traitement visuel inédit
Les chercheurs travaillant sur la prochaine génération de technologies informatiques visent à apporter de la lumière dans ce domaine, au sens propre comme au figuré...
L’espoir d’un traitement innovant pour les troubles...
Des chercheurs américains ont mis au point un stimulateur cérébral implantable de la taille d’un petit pois, une avancée technologique qui pourrait révolutionner...
Des absorbeurs solaires efficaces même à 1000°C : le pari de chercheurs
Les dispositifs solaires thermiques ont le potentiel de transformer la façon dont nous chauffons nos maisons et produisons de l’énergie à grande échelle. Une...
Un matériau promet une efficacité quantique de plus de 190 % dans les...
Des chercheurs américains ont développé un matériau qui démontre le potentiel d’augmenter considérablement l’efficacité des panneaux solaires. Ce nouveau...
Première mondiale : le magnétisme induit à température ambiante
Des chercheurs européens ont réussi à démontrer pour la toute première fois comment la lumière laser peut induire un comportement quantique à température ambiante et...
Batteries sodium : un processus 10 fois plus efficace
La transition vers des sources d’énergie plus respectueuses de l’environnement nécessite également des batteries rechargeables efficaces pour stocker cette...
Filtration : les vides nanométriques, un atout insoupçonné
Les vides, ou espaces vides, existent au sein de la matière à toutes les échelles, de l’astronomique au microscopique. Une nouvelle étude menée par des chercheurs...
Imprimer l’inconnu : quand l’IA déchiffre les matériaux...
L’impression 3D a connu un essor considérable ces dernières années, mais les matériaux plastiques utilisés par ces imprimantes pour créer des objets restent...
Des ingénieurs US conçoivent un réseau de distribution d’énergie...
L’intégration des énergies renouvelables dans le réseau électrique représente un défi majeur pour les opérateurs de réseau et les fournisseurs d’électricité...
L’hydrogène, futur de nos réservoirs de pétrole ? Sandia mène...
Les réservoirs de grès poreux, autrefois remplis de pétrole et de gaz naturel, pourraient bientôt devenir des sites de stockage pour un combustible sans carbone :...
Les montres connectées bientôt capables de mesurer les calories brûlées
La mesure précise des calories brûlées lors d’une activité physique est un défi de taille pour les appareils portables tels que les smartphones et les montres...
Première visualisation d’un état quantique à résolution atomique
Les chercheurs ont réussi à capturer pour la première fois des images à résolution atomique d’un état d’interface chiral, un phénomène quantique exotique qui...
Des nano-membranes inspirées de la nature pour un avenir durable
La conversion du dioxyde de carbone en composés utilisables grâce à l’énergie solaire, tout en produisant simultanément de l’hydrogène, est l’ambitieux...
L’IA du futur se cache dans le cerveau minuscule des papillons
Les papillons Heliconius, malgré leur cerveau minuscule, sont capables de prendre des décisions basées sur plusieurs signaux sensoriels simultanés, une prouesse que les...
57 millions $ d’économies en 15 ans : le pari renouvelable du...
L’Antarctique, continent hostile et isolé, abrite depuis longtemps des stations de recherche scientifique. Parmi elles, la station Amundsen-Scott du pôle Sud, où...
Réseaux neuronaux à pointes : l’avenir du calcul inspiré du...
Les chercheurs en neuromorphique s’efforcent de concevoir des systèmes de calcul aussi performants que le cerveau biologique, en particulier le cerveau humain, qui...
Le MIT dévoile ‘flexure’ un module polyvalent pour robots à...
Les muscles, ces merveilles de la nature, sont des actionneurs parfaits capables de transformer l’énergie en mouvement avec une puissance et une précision...
Le sable, jusqu’à 100 heures de stockage d’énergie pour un...
Le stockage d’énergie est un enjeu crucial pour l’avenir, et une solution innovante pourrait bien se trouver sous nos pieds : le sable. Grâce à sa capacité à...
L’intelligence artificielle améliore la microscopie à super...
Les méthodes computationnelles et le traitement algorithmique des données jouent un rôle crucial dans la microscopie à super-résolution. Une nouvelle approche dans ce...
PhotonWear : des photodétecteurs 50% plus sensibles grâce au silicium...
Les capteurs portables sont en passe de révolutionner le secteur de la santé, offrant des solutions innovantes pour répondre aux besoins complexes d’une population...
Comment les montagnes pourraient stocker des montagnes d’énergie...
Le stockage d’énergie propre est un enjeu majeur pour la transition vers un réseau électrique décarboné. Les montagnes, collines, falaises et plateaux pourraient...
Cellule solaire organique en tandem : 16,94% d’efficacité atteinte
Les cellules solaires organiques en tandem à quatre terminaux représentent une avancée significative dans le domaine de l’énergie solaire. Des chercheurs de...
In-Sight L38 : configurer des outils 3D avec seulement 5 à 10 images
L’inspection automatisée dans l’industrie manufacturière est en constante évolution, cherchant à améliorer la qualité et les performances. Cognex, un...
BPPflexRoll : le chaînon manquant pour une énergie hydrogène accessible
Les systèmes de piles à combustible respectueux de l’environnement, qui devraient alimenter des machines telles que les véhicules à l’avenir, sont encore...
Chaleur extrême : les ventilateurs ne suffisent plus, que faire ?
Les vagues de chaleur extrême deviennent de plus en plus fréquentes en raison du changement climatique, ce qui soulève des questions cruciales sur les moyens les plus...
Graphène et silicium : l’alliance parfaite pour...
Les matériaux innovants sont au cœur des préoccupations des chercheurs et des industriels, qui s’efforcent de développer des solutions toujours plus performantes...
Des lasers à disque pour une transmission quantique à longue portée
L’expansion de la fibre optique progresse à l’échelle mondiale, augmentant non seulement la bande passante des connexions Internet conventionnelles, mais...
400 000 modèles d’IA analysés : la clé pour réduire leur...
Le développement de l’intelligence artificielle (IA) est un facteur souvent négligé dans la lutte contre le changement climatique. Des chercheurs en informatique...
Peintures écologiques : une menace invisible pour votre santé ?
Les peintures à base d’eau sont souvent présentées comme une alternative plus écologique et moins odorante aux peintures à base de solvants. Cependant, une étude...
Adieu les lasers : l’holographie 3D depuis votre écran de...
Les chercheurs ont mis au point une nouvelle méthode d’affichage 3D en couleur qui utilise l’écran d’un smartphone plutôt qu’un laser pour créer...
3 200 mégapixels : la caméra LSST repousse les limites de...
Les scientifiques et ingénieurs du SLAC National Accelerator Laboratory du Département de l’Énergie des États-Unis et leurs collaborateurs célèbrent...
Vibrations nocives : une menace invisible pour les travailleurs du BTP
Les chercheurs de l’institut Fraunhofer ont développé un casque équipé d’un capteur d’accélération intégré destiné aux conducteurs d’engins de...