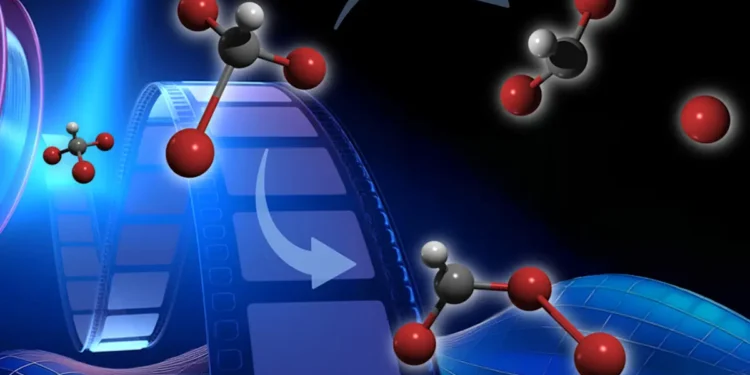
Pour la première fois, des chercheurs ont observé comment le bromoforme réarrange ses atomes en moins d’un trillionième de seconde après avoir été frappé par une impulsion ultraviolette (UV). La technique d’imagerie a permis de saisir une voie prédite depuis longtemps par laquelle la molécule nocive pour la couche d’ozone transforme sa structure lors de l’interaction avec la lumière.
L’énergie des rayons UV du soleil induit de nombreux processus chimiques sur Terre. Pour comprendre, utiliser ou atténuer les dommages causés par ces réactions chimiques souvent ultrarapides, il est essentiel de comprendre leur fonctionnement au niveau atomique. « Comment les électrons et les atomes communiquent-ils entre eux pour qu’une certaine réaction chimique se produise ? Le bromoforme est un système modèle de premier plan pour répondre à ces questions », explique Oliver Gessner, scientifique principal au Lawrence Berkeley National Laboratory (Berkeley Lab) du ministère de l’énergie.
Depuis des décennies, les chimistes du monde entier étudient la photochimie du bromoforme dans l’ultraviolet. Ce composé naturel décompose l’ozone dans l’atmosphère terrestre et est naturellement produit par le phytoplancton et les algues marines dans les océans. Selon la théorie, il subit deux processus différents sous exposition aux UV : dans la dissociation, un atome de brome se sépare du reste de la molécule ; dans l’isomérisation, les atomes se réarrangent dans une configuration différente ou isomère.
« Certains prétendent avoir observé des signatures de cet isomère, mais il a été trop éphémère pour être prouvé », a déclaré M. Gessner, qui dirige le programme des sciences atomiques, moléculaires et optiques de la division des sciences chimiques du laboratoire de Berkeley. En outre, les théories diffèrent considérablement quant à la proportion de bromoforme qui suit chaque voie.
Dans une étude publiée dans le Journal of the American Chemical Society, Gessner et ses collègues ont mis au point une expérience qui non seulement confirme cette formation d’isomères, mais détermine également la proportion de molécules de bromoforme qui subissent une dissociation et la proportion de molécules qui forment des isomères.
Les chercheurs ont d’abord excité les molécules de bromoforme gazeux avec une rafale ultra-rapide de lumière UV (longueur d’onde de 267 nanomètres), puis ils ont imagé les molécules excitées avec des impulsions électroniques ultra-courtes en utilisant l’instrument de diffraction électronique ultra-rapide relativiste du SLAC National Accelerator Laboratory. Cet instrument fait partie de la source de lumière cohérente Linac au SLAC, une installation d’utilisateurs de l’Office of Science du ministère de l’énergie.
« Les molécules décident en quelques centaines de femtosecondes de la direction qu’elles vont prendre, nous devions donc être plus rapides que cela », a ajouté M. Gessner.
Newsletter Enerzine
Recevez les meilleurs articles
Énergie, environnement, innovation, science : l’essentiel directement dans votre boîte mail.
À partir des images électroniques, les chercheurs ont pu mesurer les distances entre les atomes à l’intérieur des molécules de bromoforme et suivre l’évolution de ces distances dans le temps. L’analyse a montré qu’environ 60 % des molécules de bromoforme subissaient une isomérisation dans les 200 premières femtosecondes (1 femtoseconde = 1/1 000 000 000 000 000 de seconde) d’excitation et que cette isomérisation persistait pendant toute la durée de l’expérience de 1,1 picoseconde (1 picoseconde est égale à 1 000 femtosecondes).
« C’était vraiment passionnant de voir exactement la configuration que certains avaient prédite pour cet isomère », a indiqué M. Gessner. Les 40 % restants du bromoforme ont subi une dissociation directe. Ce résultat constitue une étape importante dans la compréhension de la photochimie du bromoforme et de la photochimie induite par les UV en général.
« La séquence des voies chimiques a un impact sur les produits chimiques finaux », a dit encore M. Gessner.
La mesure de référence d’un taux de formation d’isomères longtemps débattu permet d’affiner les théories qui prédisent ces réactions et leurs produits. En outre, l’étude démontre que la technique ultrarapide permet d’apporter des réponses claires aux questions concernant la rapidité de peuplement des isomères et leur durée de vie. Selon M. Gessner, il s’agit là d’un outil très puissant.
Légende illustration : Une voie ultrarapide prédite depuis longtemps dans la photochimie UV du bromoforme est visualisée pour la première fois par diffraction électronique résolue en temps par femtoseconde. Crédit : Melody Li, Debadarshini Mishra et Lars Hoffmann
Article : « UV-Induced Reaction Pathways in Bromoform Probed with Ultrafast Electron Diffraction » – DOI: 10.1021/jacs.4c07165