Des chercheurs du Laboratoire National Oak Ridge du Département de l’Énergie (USA) ont eu l’occasion d’employer pour la première fois la neutronographie pour scruter l’intérieur d’une batterie à l’état solide en fonctionnement et observer son électrochimie.
Leur découverte ? Les performances exceptionnelles de cette batterie découlent d’une couche extrêmement fine, à travers laquelle les atomes de lithium chargés circulent rapidement lorsqu’ils se déplacent de l’anode à la cathode pour se fondre dans un électrolyte solide.
« Nous voulons de meilleures batteries« , affirme Andrew Westover d’ORNL, co-auteur d’une étude publiée dans ACS Energy Letters avec James Browning à la Source de Neutrons de Spallation du laboratoire. « Cela signifie plus de densité énergétique, un coût réduit, une charge de batterie plus rapide et plus sûre et une durée de vie prolongée. »
Les batteries rechargeables s’appuient sur le lithium, un petit atome métallique qui se condense fermement dans l’anode chargée négativement pour maximiser la densité énergétique. Cependant, le lithium est instable avec la plupart des électrolytes – un facteur qui contribue à l’inflammabilité des batteries de smartphones, d’ordinateurs portables et de véhicules électriques qui utilisent des électrolytes liquides.
« Pour résoudre le problème de l’inflammabilité, nous voulons passer à des électrolytes solides« , précise A. Westover.
C’est là qu’intervient le lithium phosphorus oxynitride, ou LiPON, un électrolyte solide inventé à l’ORNL il y a presque 30 ans. « On n’a jamais vraiment compris pourquoi il fonctionne aussi bien« , admet A. Westover. « Nous voulons faire fonctionner ce qui marche avec le LiPON à une échelle beaucoup plus grande. Mais nous devons d’abord le comprendre. »
Des travaux antérieurs ont montré que l’interface solide-électrolyte, ou SEI – une couche qui se forme pour protéger et stabiliser la batterie à l’état solide – est essentielle à sa capacité de charge et de décharge répétée. Dans ce cas, l’interface est un gradient chimique composé d’une couche riche en lithium dont le contenu en lithium diminue à mesure qu’elle se fond dans le LiPON pur.
« Dans une batterie normale, une interface se forme entre l’électrolyte et l’électrode de travail« , explique Browning. « Au fil du temps, à mesure que vous faites fonctionner une batterie – charge et décharge – ce matériau peut changer de composition et d’épaisseur. »
« Si vous avez une bonne SEI, votre batterie fonctionne. Si vous avez une mauvaise SEI, elle ne fonctionne pas« , souligne A. Westover. La raison pour laquelle la capacité de la batterie de votre téléphone portable diminue lentement année après année est que votre SEI se dilate et consomme votre électrolyte dans la batterie à base de liquide.
Dans une batterie à l’état solide à base de LiPON, cependant, une mince couche de SEI se forme pour passiver le lithium, le rendant non réactif, et ne grandit pas comme la SEI dans une batterie traditionnelle.
Newsletter Enerzine
Recevez les meilleurs articles
Énergie, environnement, innovation, science : l’essentiel directement dans votre boîte mail.
Les scientifiques ont associé la neutronographie à l’électrochimie pour mesurer cette interface stable entre le LiPON et le lithium pour la première fois. Elle était aussi fine que 7 nanomètres. « Nous avons découvert avec cette étude que la couche formée est d’environ 70 atomes d’épaisseur« , déclare A. Westover. « Ce travail démontre qu’il est possible de créer des interfaces dans les batteries à l’état solide qui sont minces et offrent d’excellentes performances.«
Cette petite échelle, combinée à l’état solide des matériaux, a poussé les chercheurs à utiliser des neutrons pour regarder à l’intérieur de la batterie.
« Avant la découverte des rayons X, on ne pouvait pas regarder sous la peau pour voir les os à l’intérieur d’un corps. Il fallait ouvrir la peau« , explique A. Westover. « Jusqu’à présent, c’est essentiellement l’approche que la plupart des gens ont utilisée pour examiner les interfaces dans les batteries. Dans ce cas, l’échelle est trop petite pour ouvrir quoi que ce soit. Nous avions besoin d’un outil qui nous permette de traverser le matériau, de le sonder de manière non destructive à cette échelle et de comprendre ce qui se passe à l’interface. C’est là que la neutronographie est intervenue.«
L’association de la neutronographie à l’électrochimie a accéléré la compréhension de l’interface entre le métal lithium et les électrolytes solides dans les batteries à l’état solide.
« Cette combinaison de techniques ouvre la porte pour nous permettre d’examiner tout le spectre des matériaux d’électrolytes à l’état solide et de déterminer lesquels permettront d’obtenir des batteries à haute énergie et à charge rapide« , déclare A. Westover. « Nous avons déjà commencé la version 2.0, où nous examinons un autre type d’électrolytes solides et commençons à comprendre à quoi ils ressemblent. »
Il ajoute : « De nouveaux matériaux doivent être inventés qui ont cette stabilité. » La conception des futures batteries haute performance en dépendra.
Le titre de l’article est « Mesure in situ des interfaces enterrées électrolyte-électrode pour les batteries à l’état solide avec une précision de niveau nanométrique. »
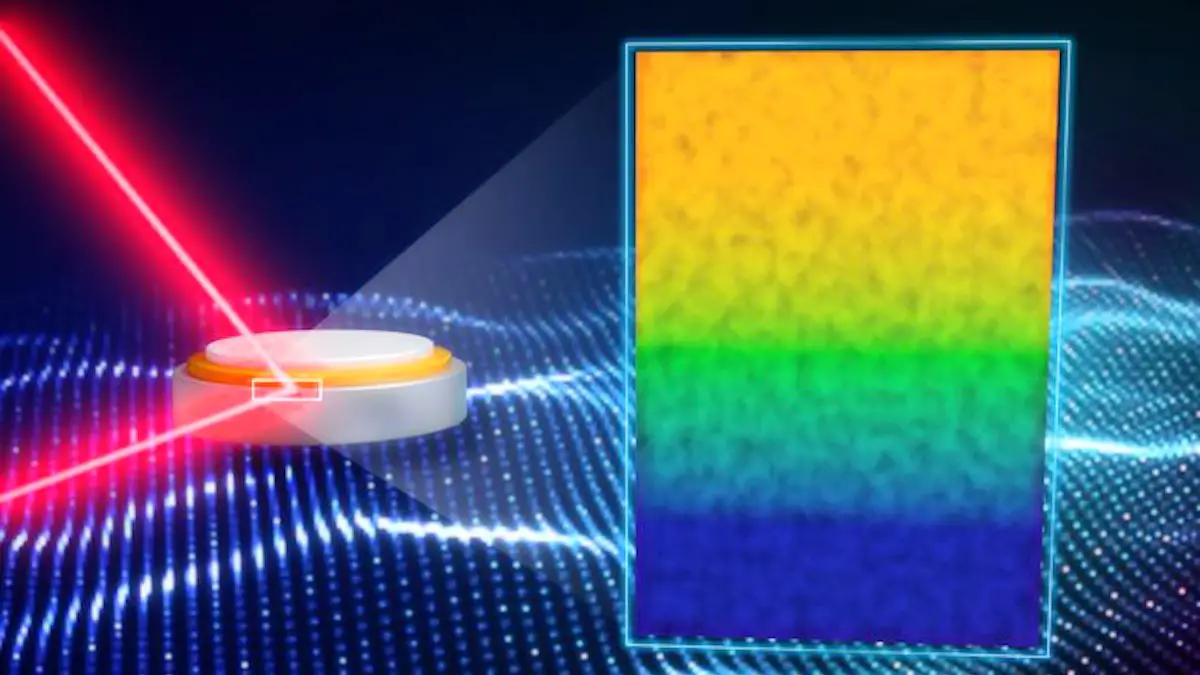
Illustration – légende : Dans une batterie à l’état solide, le lithium métal réactif (bleu) peut coexister de manière stable avec un électrolyte solide appelé LiPON (jaune) lorsqu’une interphase (verte), d’une épaisseur d’environ 70 atomes, se forme. Crédit / Jill Hemman/ORNL, Département de l’énergie des États-Unis