Lorsque l’on pense au fluorure de sodium, couramment utilisé dans de nombreux dentifrices, c’est généralement pour sa capacité à protéger contre les caries. Pourtant, ce composé de fluor a des utilisations bien plus étonnantes.
Les scientifiques du Département de l’Énergie des États-Unis (DOE) et du Laboratoire national d’Argonne ont récemment découvert une utilisation du fluorure en tant qu’électrolyte pouvant préserver les performances des batteries de nouvelle génération.
« Une nouvelle génération prometteuse de batteries pour véhicules électriques se profile à l’horizon », déclare Zhengcheng (John) Zhang, chef de groupe au sein de la division des sciences et de l’ingénierie chimiques d’Argonne.
Les batteries non-lithium-ion : une énergie deux fois plus puissante
Les batteries non-lithium-ion présentent une énergie deux fois supérieure ou plus, par volume ou par poids, comparée aux batteries lithium-ion. Ces dernières pourraient un jour propulser des camions sur de longues distances et même des avions. Le principal défi reste toutefois la diminution rapide de leur haute densité énergétique lors des cycles répétés de charge et de décharge.
« Les batteries au lithium métallique avec notre électrolyte à cation fluoré pourraient considérablement stimuler l’industrie du véhicule électrique. Et l’utilité de cet électrolyte s’étend sans aucun doute à d’autres types de systèmes de batteries avancés au-delà du lithium-ion. » – John Zhang, chef de groupe dans la division des sciences et de l’ingénierie chimiques.
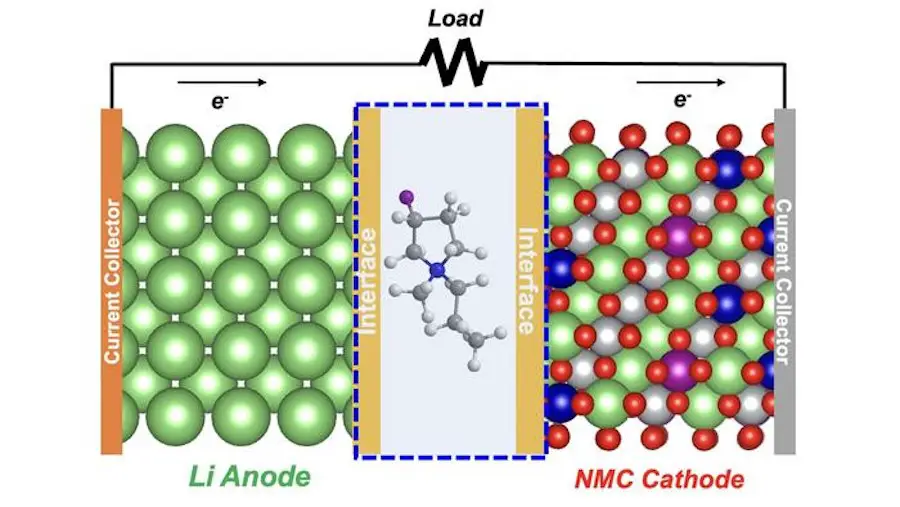
La solution : un électrolyte au fluorure
Les chercheurs se sont penchés sur l’électrolyte, ce liquide par lequel les ions lithium se déplacent entre la cathode et l’anode pendant la charge et la décharge. Dans les batteries au lithium métallique, l’électrolyte ne forme pas de couche protectrice adéquate sur la surface de l’anode pendant les premiers cycles. Cette couche, également appelée interface solide-électrolyte (SEI), joue le rôle de gardien, permettant aux ions lithium de circuler librement dans l’anode pour charger et décharger la batterie.
C’est en remplaçant l’hydrogène par du fluor dans la structure annulaire de la partie cation de l’électrolyte que l’équipe est parvenue à maintenir des performances élevées sur plusieurs centaines de cycles dans une cellule de test au lithium métallique.
De la théorie à la pratique : le rôle de la superinformatique
Newsletter Enerzine
Recevez les meilleurs articles
Énergie, environnement, innovation, science : l’essentiel directement dans votre boîte mail.
Pour mieux comprendre le mécanisme à l’échelle atomique, l’équipe a recours aux ressources informatiques de haute performance du Argonne Leadership Computing Facility (ALCF). Selon Zhang, les simulations réalisées sur le supercalculateur Theta de l’ALCF ont révélé que les cations fluor se collent et s’accumulent sur les surfaces des anodes et des cathodes avant tout cycle de charge-décharge.
Ensuite, pendant les premiers stades du cyclage, une couche SEI résiliente se forme, supérieure à ce qui est possible avec les électrolytes précédents.
En synthèse
La nouvelle électrolyte de l’équipe offre de nombreux autres avantages. Elle est économique, car elle peut être produite avec une pureté et un rendement extrêmement élevés en une seule étape. Elle est respectueuse de l’environnement, car elle utilise beaucoup moins de solvant, qui est volatile et peut libérer des contaminants. Et elle est plus sûre car elle n’est pas inflammable.
Pour une meilleure compréhension
Qu’est-ce qu’un électrolyte au fluorure ?
Quels sont les avantages d’une batterie non-lithium-ion ?
Comment fonctionne le nouveau processus d’électrolyte au fluorure ?
Quel est le rôle de l’interface solide-électrolyte (SEI) ?
Un article sur cette recherche a été publié dans Nature Communications. Outre M. Zhang, les auteurs d’Argonne sont Qian Liu, Wei Jiang, Jiayi Xu, Zhenzhen Yang, Doo-Joo Yoo, Krzysztof Z. Pupek et Cong Liu. Parmi les autres contributeurs figurent Chongmin Wang et Yaobin Xu du Pacific Northwest National Laboratory et Kang Xu du U.S. Army Research Laboratory.