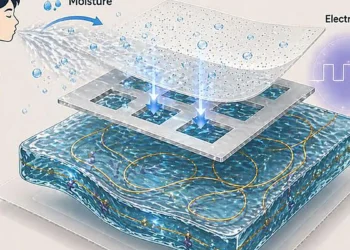
Au sein des tissus, les cellules sont intégrées dans des structures complexes et tridimensionnelles appelées matrice extracellulaire. Leurs interactions biomécaniques jouent un rôle crucial dans de nombreux processus biologiques. Des scientifiques de l’Institut Max Planck pour la science de la lumière (MPL) ont désormais développé un nouveau système lab-on-a-chip basé sur des structures d’hydrogel intelligent, qui permet d’appliquer des forces de pression précises sur les microenvironnements cellulaires. La méthode récemment présentée pourrait trouver des applications futures dans le diagnostic médical des troubles mécaniques des tissus vivants.
Biomécanique des cellules simulée par une méthode lab-on-a-chip
Le remodelage mécanique du microenvironnement extracellulaire joue un rôle crucial dans les processus biologiques tels que le développement et le maintien de l’équilibre physiologique (homéostasie) et la cicatrisation. Le reproduire en laboratoire peut fournir des informations sur les causes des changements pathologiques. Cependant, les méthodes instrumentales précédentes ne pouvaient pas être intégrées dans des systèmes lab-on-a-chip et n’offraient qu’une précision limitée.
L’équipe dirigée par le Dr Katja Zieske, responsable du groupe de recherche indépendant « Biophysique moléculaire & matière vivante » au MPL, présente maintenant une nouvelle méthode qui peut être utilisée pour simuler des perturbations mécaniques contrôlées spatialement et temporellement de réseaux de polymères biologiques sur un système lab-on-a-chip. Les processus biologiques survenant lors de telles perturbations peuvent ainsi être examinés au microscope.
Des hydrogels intelligents comme micromachines
Les scientifiques utilisent des microstructures d’hydrogel intelligent. Ces matériaux puissants sont constitués de polymères qui répondent à des stimuli tels que la lumière ou la température en modifiant leur structure. Selon le stimulus, ils se contractent ou se dilatent. Les chercheurs du MPL ont tiré parti de ces propriétés pour exercer des forces biomécaniques spécifiquement définies sur des réseaux de polymères biologiques comme le collagène. De plus, les scientifiques ont pu évaluer la compatibilité du système avec les cellules vivantes.
Dans un premier temps, l’équipe de Zieske a produit et optimisé des microstructures d’hydrogel thermosensibles dans des chambres de flux. L’expansion des microstructures d’hydrogel a été testée sous stimulation thermique contrôlée dans le temps pour comprimer divers réseaux moléculaires, tels que le Matrigel, un mélange protéique gélifié, et un réseau de collagène. Après compression, la déformation associée a été mesurée.
Alors que le Matrigel se déformait plastiquement, le collagène se relaxait de manière élastique. En imitant les forces de pression cellulaires à l’aide de microstructures d’hydrogel intelligent, l’équipe de Zieske a développé un nouveau système polyvalent à des fins de recherche. Les études futures pourraient se concentrer sur le remodelage de la matrice extracellulaire ainsi que sur les effets des forces mécaniques sur son microenvironnement cellulaire, tant dans des contextes physiologiques que pathologiques.
Notre méthode nous permet de générer des forces mécaniques avec une grande précision spatiale et temporelle, et d’enregistrer leurs effets sur les systèmes biologiques. Dans le collagène, nous avons pu détecter des changements déclenchés par ces forces même à des distances de centaines de micromètres en suivant des microsphères fluorescentes, explique Vicente Salas-Quiroz, premier auteur du travail présenté.
Notre vision est de développer des microstructures intelligentes pour le diagnostic médical afin de contribuer à un système de santé durable – par exemple, dans l’étude de systèmes de modèles cellulaires 3D comme les modèles de cancer et les modèles de formation de vaisseaux sanguins. Les microstructures d’hydrogel intelligent dans les systèmes lab-on-a-chip pourraient servir de micromachines à l’avenir pour manipuler des modèles de tissus à l’échelle micrométrique. Nous voyons ici un grand potentiel pour une utilisation diagnostique, ajoute Zieske.
Article : « Stimulus-induced mechanical compaction of biological polymer networks via smart hydrogel microstructures » – Journal : Lab on a Chip – Méthode : Experimental study – Sujet : Cells – DOI : 10.1039/D5LC00477B
Source : Max Planck Institute
Newsletter Enerzine
Recevez les meilleurs articles
Énergie, environnement, innovation, science : l’essentiel directement dans votre boîte mail.