La médecine contemporaine s’efforce de répondre à une question centrale : comment adapter les soins aux besoins spécifiques de chaque individu, tout en assurant un suivi continu et non invasif ? La réponse pourrait résider dans des dispositifs capables de surveiller en temps réel des biomarqueurs essentiels. Une équipe d’ingénieurs californiens a franchi une étape significative dans ce domaine grâce à une technologie innovante.
Des nanoparticules imprimées pour un suivi médical personnalisé
Une méthode récente mise au point par des chercheurs de l’Institut de technologie de Californie (Caltech) repose sur l’impression par jet d’encre de réseaux constitués de nanoparticules spéciales. Ces dernières permettent la fabrication en série de capteurs portables destinés à analyser la sueur humaine. Leur particularité réside dans leur capacité à mesurer divers biomarqueurs tels que des vitamines, hormones, métabolites ou encore des médicaments. Cette innovation offre aux patients et à leurs praticiens un outil performant pour suivre en continu les fluctuations des niveaux moléculaires.
Les applications pratiques ont déjà été validées dans plusieurs contextes cliniques. Des capteurs intégrant ces nanoparticules ont ainsi été employés pour surveiller les métabolites chez des personnes atteintes de long COVID, ainsi que les concentrations de médicaments anticancéreux chez des patients suivis au City of Hope, un centre médical situé à Duarte, en Californie. «.
Structure et fonctionnement des nanoparticules
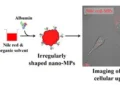
Les nanoparticules développées par l’équipe de Gao sont qualifiées de nanoparticules cœur-coquille cubiques. Leur conception repose sur un procédé minutieux. Les cubes sont formés dans une solution contenant la molécule cible, comme la vitamine C. Lorsque les monomères s’auto-assemblent pour former un polymère, la molécule cible est piégée à l’intérieur des nanoparticules cubiques. Par la suite, un solvant est utilisé pour extraire sélectivement ces molécules, laissant derrière elles une coquille polymérique imprimée moléculairement, percée de cavités correspondant exactement à la forme de la molécule cible. Ces cavités agissent comme des anticorps artificiels, reconnaissant uniquement des structures spécifiques.
Dans cette étude, les chercheurs ont associé ces polymères spécialement conçus à un noyau de nickel hexacyanoferrate (NiHCF). Ce matériau peut être oxydé ou réduit sous l’effet d’une tension électrique lorsqu’il entre en contact avec la sueur ou d’autres fluides corporels. Reprenons l’exemple de la vitamine C : tant que les cavités en forme de vitamine C restent inoccupées, le fluide interagit avec le noyau de NiHCF, générant un signal électrique. En revanche, lorsque des molécules de vitamine C se fixent dans ces cavités, elles bloquent l’accès du fluide au noyau, affaiblissant le signal électrique. L’intensité de ce dernier reflète alors directement la concentration de vitamine C présente.

«Ce noyau est primordial», souligne Gao. «Le noyau de nickel hexacyanoferrate est extrêmement stable, même dans les fluides biologiques, ce qui rend ces capteurs idéaux pour des mesures à long terme», ajoute-t-il.
Applications multiples et production en série
Ces nouvelles nanoparticules cœur-coquille se distinguent par leur polyvalence. Elles servent à imprimer des réseaux de capteurs capables de mesurer simultanément les niveaux de plusieurs acides aminés, métabolites, hormones ou médicaments dans la sueur ou d’autres fluides corporels. Dans les travaux décrits dans l’article scientifique, les chercheurs ont produit des nanoparticules capables de se lier à la vitamine C, mais aussi à des molécules telles que le tryptophane, un acide aminé, et la créatinine, un biomarqueur couramment analysé pour évaluer la fonction rénale. Toutes ces nanoparticules ont été combinées en un seul capteur, puis fabriquées en série. Ces trois molécules suscitent un intérêt particulier dans les études portant sur les patients souffrant de long COVID.
De manière similaire, des capteurs portables basés sur des nanoparticules ont été élaborés pour cibler trois médicaments anticancéreux différents. Testés sur des patients atteints de cancer au City of Hope, ils ont permis de surveiller à distance les concentrations de ces traitements dans l’organisme à tout moment. «En illustrant le potentiel de cette technologie, il a été possible de personnaliser les doses non seulement pour le traitement du cancer, mais aussi pour de nombreuses autres pathologies», précise Wei Gao.
Les chercheurs ont également démontré que ces nanoparticules pouvaient être utilisées pour imprimer des capteurs implantables juste sous la peau, afin de surveiller précisément les niveaux de médicaments dans le corps.
En synthèse
Les travaux menés par l’équipe de Caltech représentent une contribution majeure au développement de dispositifs médicaux portables et implantables. Grâce à leur conception ingénieuse, ces capteurs offrent des capacités inédites pour le suivi en temps réel de biomarqueurs clés. Bien qu’ils aient déjà prouvé leur efficacité dans des contextes cliniques variés, leur potentiel reste vaste. En permettant une surveillance continue et non invasive, ces technologies préfigurent un avenir où les soins médicaux seront davantage adaptés aux besoins individuels des patients.
Newsletter Enerzine
Recevez les meilleurs articles
Énergie, environnement, innovation, science : l’essentiel directement dans votre boîte mail.
Pour une meilleure compréhension
Qu’est-ce qu’un biomarqueur ?
Un biomarqueur désigne toute substance ou caractéristique mesurable dans le corps humain qui fournit des informations sur l’état de santé d’un individu. Il peut s’agir d’une molécule spécifique, comme une hormone ou un métabolite, ou encore d’un paramètre physiologique.
Comment fonctionne le principe de reconnaissance moléculaire ?
Le principe repose sur la création de cavités dans une coquille polymérique, dont les formes correspondent exactement à celles des molécules cibles. Ces cavités agissent comme des récepteurs hautement sélectifs, reconnaissant uniquement les molécules ayant une structure spécifique.
Quelles sont les principales applications des capteurs développés ?
Ces capteurs peuvent être utilisés pour surveiller des vitamines, métabolites, hormones ou médicaments dans la sueur ou d’autres fluides corporels. Ils trouvent des applications dans le suivi de maladies chroniques, comme le long COVID, ainsi que dans la gestion des traitements anticancéreux.
Pourquoi le nickel hexacyanoferrate est-il utilisé ?
Ce matériau présente une stabilité exceptionnelle dans les fluides biologiques. Sa capacité à générer des signaux électriques sous l’effet d’une tension en fait un composant idéal pour des capteurs durables et fiables.
Peut-on envisager d’autres utilisations futures pour ces capteurs ?
Oui, leur polyvalence laisse entrevoir des applications dans de nombreux domaines, notamment pour le suivi de maladies neurodégénératives, la gestion des troubles métaboliques ou encore l’optimisation des thérapies médicamenteuses.
Légende illustration : Des nanoparticules sélectives aux molécules imprimables permettent la production en masse de biocapteurs portables. Crédit : Caltech
Article : « Printable molecule-selective core–shell nanoparticles for wearable and implantable sensing » – DOI : s41563-024-02096-4
Source : Caltech