La production d’ammoniac, un composé chimique largement utilisé dans divers secteurs industriels, fait face à des défis environnementaux majeurs en raison de son impact significatif sur les émissions de carbone. Une équipe d’ingénieurs de l’Université de l’Illinois à Chicago, dirigée par le professeur Meenesh Singh, a développé un nouveau procédé de synthèse d’ammoniac prometteur, répondant à plusieurs critères de durabilité.
Un procédé innovant basé sur le lithium
Le procédé, appelé synthèse d’ammoniac médiée par le lithium, combine du diazote et un fluide donneur d’hydrogène, comme l’éthanol, avec une électrode de lithium chargée. Contrairement aux méthodes conventionnelles nécessitant des températures et des pressions élevées pour dissocier les molécules de diazote, les atomes d’azote adhèrent au lithium, puis se combinent avec l’hydrogène pour former la molécule d’ammoniac.
L’un des avantages majeurs de cette réaction est qu’elle fonctionne à basse température. De plus, elle est régénérative, restaurant les matériaux d’origine à chaque cycle de production d’ammoniac. Selon le professeur Singh, « il y a une symphonie dans cette réaction, en raison du processus cyclique. Ce que nous avons fait, c’est de mieux comprendre cette symphonie et d’essayer de la moduler de manière très efficace, afin de créer une résonance et de la faire avancer plus rapidement. »
Des résultats prometteurs en termes d’efficacité et de coût
Les résultats obtenus par l’équipe du professeur Singh figurent parmi les premiers à atteindre des niveaux de sélectivité et d’utilisation d’énergie répondant aux normes du Département de l’Énergie des États-Unis pour la production d’ammoniac à l’échelle industrielle. Si le procédé était mis à l’échelle, il permettrait de produire de l’ammoniac à environ 450 dollars par tonne, soit 60 % moins cher que les approches précédentes basées sur le lithium et d’autres méthodes vertes proposées.
De plus, le procédé peut être rendu encore plus écologique en l’alimentant avec de l’électricité provenant de panneaux solaires ou d’autres sources renouvelables, et en utilisant de l’air et de l’eau pour la réaction. Le professeur Singh souligne également que l’ammoniac produit pourrait servir de vecteur d’hydrogène, facilitant ainsi le transport et l’utilisation de l’hydrogène comme carburant.
Vers une mise à l’échelle industrielle
Actuellement, les scientifiques collaborent avec la société General Ammonia Co. pour piloter et mettre à l’échelle leur procédé de synthèse d’ammoniac médiée par le lithium dans une usine de la région de Chicago. L’Office de gestion de la technologie de l’UIC a déposé un brevet pour ce procédé innovant.
Cette percée dans la production d’ammoniac ouvre le chemin à une industrie chimique plus durable et respectueuse de l’environnement, tout en offrant de nouvelles perspectives pour l’utilisation de l’hydrogène comme carburant propre.
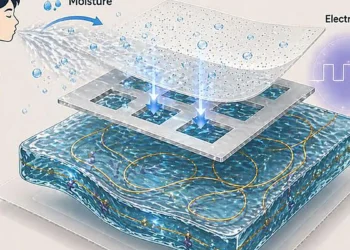
Légende illustration : Cet art graphique illustre la conversion de N2 en ammoniac par l’intermédiaire du lithium. On y voit une symphonie de réactions se produisant sur un lithium électro-déposé (tuiles noires). Sous haute pression, l’azote (ajout de blocs bleus) est chimisorbé sur le lithium, suivi d’une protonation (ajout de blocs blancs) pour former NHx, ce qui conduit finalement à l’ammoniac et à la récupération du lithium. Le processus cyclique crée un rythme catalytique produisant de l’ammoniac. Cette recherche met en évidence l’importance de la pression et du potentiel dans le contrôle de la structure et de la stabilité de l’interface solide-électrolyte pour la synthèse de l’ammoniac. Crédit : Crystal Price & Joseph Gauthier, Texas Tech University; Meenesh Singh, University of Illinois Chicago
Newsletter Enerzine
Recevez les meilleurs articles
Énergie, environnement, innovation, science : l’essentiel directement dans votre boîte mail.