Les biofilms sont des films visqueux composés de micro-organismes et d’autres substances qui peuvent se développer sur un large éventail de surfaces, y compris les implants médicaux, les dents et même les rochers dans les rivières et les ruisseaux. Ces biofilms sont maintenus ensemble par une matrice de substances polymériques extracellulaires qui offrent une protection aux micro-organismes contre les défis environnementaux, tels que les antibiotiques.
« Les biofilms peuvent être très difficiles à éliminer et posent des défis importants car ils peuvent être très résistants aux traitements, ce qui les rend responsables de nombreuses infections chroniques, en particulier celles liées aux implants médicaux« , explique Mengmeng Sun, chercheur au département d’ingénierie mécanique et d’automatisation de l’université chinoise de Hong Kong.
Lutter contre les biofilms grâce aux micromachines
Afin de lutter contre la formation de biofilms au sein de structures tubulaires de petite taille, une étude récente publiée dans Advanced Intelligent Systems a présenté le développement de micromachines à base d’hydrogel magnétique. Ces dernières sont conçues pour accomplir deux tâches cruciales : perturber mécaniquement le biofilm et contrôler la libération d’agents antibiotiques.
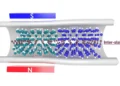
Ces micromachines doubles fonction aident à démanteler les biofilms. La clé de leur fonctionnement réside dans le matériau unique dont elles sont faites : un hydrogel magnétique thermosensible. Grâce à leurs propriétés magnétiques, les micromachines peuvent être dirigées avec précision vers l’endroit souhaité à l’aide de champs magnétiques externes, après quoi elles peuvent exercer des forces mécaniques spécifiques pour aider à briser manuellement le biofilm, le rendant ainsi plus susceptible d’être traité avec des agents chimiques.

Fonctionnalités des micromachines à base d’hydrogel
« L’un des avantages des micromachines est qu’elles peuvent se déplacer de différentes manières. Elles peuvent tourner de façon circulaire ou osciller d’avant en arrière« , explique M. Sun, l’un des auteurs de l’étude. « Cela leur permet également d’accéder aux biofilms situés dans des zones difficiles d’accès, telles que les espaces étroits ou les tubes utilisés dans de nombreux dispositifs médicaux et implants. »
Ces micromachines ont été conçues pour contenir de minuscules compartiments d’hydrogel capables de stocker des agents antibactériens. « Lorsque l’hydrogel est chauffé au-dessus de sa température de solution critique inférieure d’environ 32 °C, il tend à expulser le contenu liquide qu’il transporte« , précise l’équipe dans leur publication. « De plus, les hydrogels sont doux, humides et biocompatibles, ce qui en fait d’excellents candidats pour les applications biomédicales. »
Newsletter Enerzine
Recevez les meilleurs articles
Énergie, environnement, innovation, science : l’essentiel directement dans votre boîte mail.
Micromachines : des désinfectants rapides et efficaces
Les micromachines ont été testées sur des biofilms d’E. coli et de B. cereus cultivés en laboratoire dans des tubes courbes et des tubes de microcentrifugation. « Pour tester notre nouvelle technologie, nous avons cultivé des biofilms en laboratoire et les avons exposés aux micromachines« , a déclaré M. Sun, « et nous avons constaté qu’elles étaient capables de détruire les biofilms et de tuer 99,3 % des cellules dormantes en seulement cinq minutes de traitement« .
Les chercheurs pensent que cette approche pourrait conduire à des traitements plus efficaces des infections liées au biofilm, en particulier celles qui se produisent dans les implants tubulaires. Cette technologie pourrait permettre d’améliorer les résultats des traitements dans diverses applications, notamment les implants biomédicaux et d’autres dispositifs médicaux.
Toutefois, il reste des obstacles à surmonter avant que les micromachines puissent être utilisées dans un hôpital ou dans un cadre clinique. « L’un des principaux problèmes auxquels nous devons réfléchir est de savoir comment les débris du biofilm peuvent être récupérés après avoir été détruits par les micromachines« , a ajouté M. Sun.
« Nous continuons à travailler sur le développement de nouveaux matériaux et systèmes afin d’optimiser les performances des micromachines« , a déclaré M. Sun. « Une fois que les conditions seront réunies, les chercheurs commenceront d’autres expériences sur les animaux. Ils espèrent qu’elles pourront être utilisées pour traiter un large éventail d’infections liées aux biofilms.«
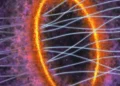
Légende image principale : des micromachines d’hydrogel magnétique brisent les biofilms et libèrent des antibiotiques, luttant ainsi contre les infections par biofilm associées aux dispositifs médicaux.
Référence : MengMeng Sun, Tony K. F. Chan, Li Zhang, et al, Magnetic Hydrogel Micromachines with Active Release of Antibacterial Agent for Biofilm Eradication. Advanced Intelligent Systems (2023), DOI : 10.1002/aisy.202300092