Les canaux ioniques sont des passages étroits qui jouent un rôle essentiel dans de nombreux processus biologiques. Pour modéliser le mouvement des ions à travers ces espaces restreints, il est nécessaire de fabriquer des pores à des échelles de longueur très petites. Les régions les plus étroites des canaux ioniques peuvent ne mesurer que quelques ångströms de large, environ la taille d’atomes individuels, ce qui rend leur fabrication reproductible et précise un défi majeur de la nanotechnologie moderne.
Dans une étude publiée dans Nature Communications, des chercheurs de l’université d’Osaka ont relevé ce défi en utilisant un réacteur électrochimique miniature pour créer des pores ultra-petits approchant les dimensions subnanométriques.
Dans les cellules biologiques, les ions entrent et sortent par des canaux dans les membranes cellulaires. Ce flux ionique est à la base de la génération de signaux électriques, comme les impulsions nerveuses qui déclenchent la contraction musculaire. Les canaux eux-mêmes sont constitués de protéines et peuvent avoir des régions étroites de l’ordre de l’ångström. Des changements de conformation de ces protéines en réponse à des stimuli externes ouvrent et ferment les canaux.
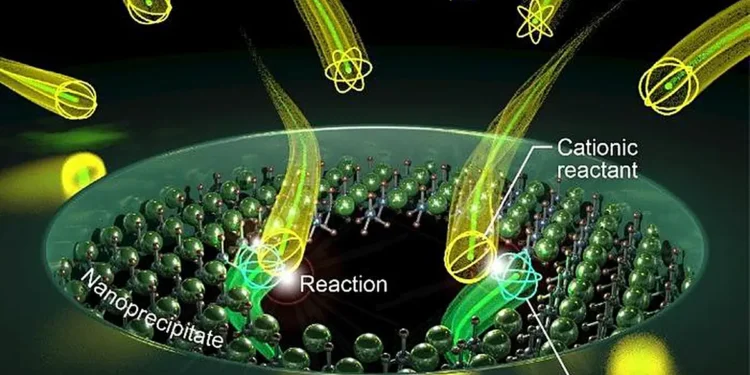
Inspirés par ces systèmes biologiques, l’équipe de recherche a développé un analogue à l’état solide permettant la formation de pores subnanométriques approchant les dimensions des canaux ioniques biologiques. Un pore à l’échelle nanométrique a été utilisé comme réacteur pour former les pores subnanométriques. Tout d’abord, le nanopore a été créé dans une membrane de nitrure de silicium. L’application d’une tension négative à travers la membrane a induit une réaction dans le pore produisant un précipité. Le précipité a grandi jusqu’à bloquer complètement le pore. L’application d’une tension positive sur la membrane a provoqué la dissolution du précipité et la réouverture de voies conductrices à l’intérieur du pore.
« Nous avons pu répéter ce processus d’ouverture et de fermeture des centaines de fois sur plusieurs heures », explique le premier auteur Makusu Tsutsui. « Cela démontre que le schéma réactionnel est robuste et contrôlable. »
L’équipe a mesuré le courant ionique à travers la membrane. Des pics de courant ont été observés, similaires à ceux des canaux biologiques. L’analyse de ces pics suggère que la formation du précipité correspond le mieux à la formation de nombreux pores subnanométriques au sein du nanopore.
« Nous avons pu varier le comportement et la taille effective des pores ultra-petits en modifiant la composition et le pH des solutions réactives », rapporte Tomoji Kawai, auteur principal. « Cela a permis le transport sélectif d’ions de tailles effectives différentes à travers la membrane en ajustant les tailles des pores ultra-petits. »
Le nouveau schéma réactionnel permet la formation de nombreux pores ultra-petits au sein d’un seul nanopore. Cette approche fournit un outil puissant pour réaliser des études fondamentales sur le transport des ions et des fluides dans des espaces très confinés aux échelles biologiques. Le système de membrane à commande chimique promet des applications dans des technologies émergentes telles que la détection de molécules uniques (par exemple, l’utilisation de nanopores pour séquencer l’ADN), l’informatique neuromorphique (utilisant des pics électriques pour imiter le comportement des neurones biologiques) et les nanoréacteurs (créant des conditions réactionnelles uniques grâce au confinement).
Article : Chemistry-driven autonomous nanopore membranes – Journal : Nature Communications – Méthode : Experimental study – DOI : Lien vers l’étude
Source : Osaka U.
Newsletter Enerzine
Recevez les meilleurs articles
Énergie, environnement, innovation, science : l’essentiel directement dans votre boîte mail.