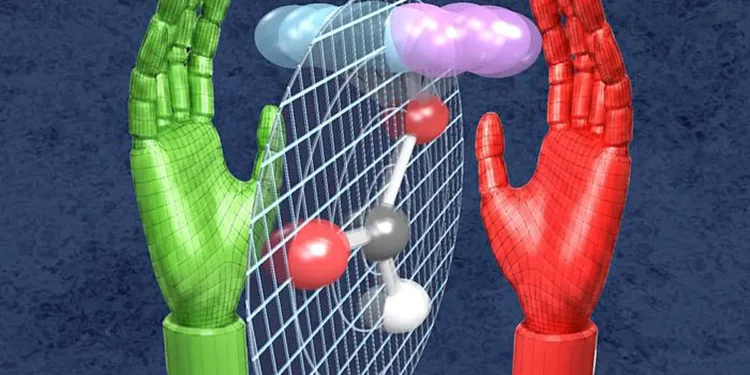
Les manuels de chimie traditionnels présentent une image bien rangée : les atomes dans les molécules occupent des positions fixes, reliés par des tiges rigides. Une molécule comme l’acide formique (acide méthanoïque, HCOOH) est imaginée comme bidimensionnelle – plate comme une feuille de papier. Mais la physique quantique raconte une histoire différente. En réalité, la nature résiste à la rigidité et force même les structures les plus simples dans la troisième dimension.
Des chercheurs dirigés par le professeur Reinhard Dörner de l’Institut de physique nucléaire de l’Université Goethe ont désormais déterminé la structure spatiale précise de la molécule d’acide formique « plate » en utilisant un faisceau de rayons X de la source de rayonnement synchrotron PETRA III au centre d’accélération DESY de Hambourg. Ils ont collaboré avec des collègues des universités de Kassel, Marbourg et du Nevada, de l’Institut Fritz Haber et de l’Institut Max Planck de physique nucléaire.
Pour ce faire, ils ont utilisé deux effets qui se produisent lorsque le rayonnement X frappe une molécule. Premièrement, le rayonnement éjecte plusieurs électrons de la molécule (effet photoélectrique et effet Auger). En conséquence, les atomes deviennent si fortement chargés que la molécule éclate dans une explosion (explosion de Coulomb). Les scientifiques ont réussi à mesurer ces processus séquentiellement, même s’ils se produisent en quelques femtosecondes – des millionièmes de milliardième de seconde.
À cette fin, ils ont utilisé un appareil inventé à l’Université Goethe et continuellement perfectionné depuis : le microscope à réaction COLTRIMS. Sur la base des données de mesure, ils ont ensuite pu calculer la géométrie originelle de la molécule d’acide formique. Le résultat : les deux atomes d’hydrogène de l’acide formique oscillent légèrement d’avant en arrière, ce qui signifie que la molécule n’est pas plate.
« Dans le monde quantique, les noyaux atomiques ne sont pas de minuscules sphères qui restent fixes en place. Ils ressemblent plus à des nuages vibrants. Même si nous refroidissons une molécule au zéro absolu, ce tremblement – le mouvement dit de point zéro – ne s’arrête jamais. » explique Reinhard Dörner.
La conséquence est radicale : un noyau atomique n’a pas d’emplacement exact, seulement une probabilité d’être trouvé à un endroit particulier. En un sens, il est « un peu partout ». En conséquence, une molécule d’acide formique est effectivement tridimensionnelle à presque chaque instant.
Il ajoute : « Grâce à ce petit pas dans la troisième dimension, la molécule perd sa symétrie et ne peut plus être superposée à son image miroir – comme nos mains gauche et droite. L’acide formique est chiral – il a une forme gauche la moitié du temps et une forme droite l’autre moitié. »
En chimie, deux formes chirales de ce type – les énantiomères – peuvent avoir des effets complètement différents : alors qu’une forme d’une molécule peut agir comme un médicament, son image miroir peut être inefficace. Normalement, cette chiralité provient de la structure fixe d’une molécule.
Et de conclure : « Comme nous avons pu le montrer avec l’exemple de l’acide formique, le tremblement quantique seul peut générer deux réalités miroir différentes à partir d’une molécule symétrique. Cela signifie que la chiralité – une propriété importante de la vie – ne provient pas ici du plan statique de la molécule, mais uniquement du tremblement incessant du monde quantique. Plus généralement, nos résultats avec l’acide formique montrent que la géométrie n’est pas une propriété statique mais un événement dynamique, et qu’une molécule plate n’est en réalité que la moyenne de ses atomes qui tremblent dans toutes les directions. »
Article : Probing Instantaneous Single-Molecule Chirality in the Planar Ground State of Formic Acid. – Journal : Physical Review Letters – Méthode : Experimental study – DOI : Lien vers l’étude
Newsletter Enerzine
Recevez les meilleurs articles
Énergie, environnement, innovation, science : l’essentiel directement dans votre boîte mail.
Source : Goethe U. Frankfurt