Dans un laboratoire de Caltech, une équipe de chercheurs a marqué une étape décisive en médecine régénérative. Leur méthode, baptisée DISP (pour Deep Tissue In Vivo Sound Printing), permet d’imprimer des structures polymériques directement à l’intérieur des tissus vivants, grâce à l’utilisation d’ultrasons. Cette technique, détaillée dans une étude récente, offre des perspectives inédites pour le traitement de pathologies complexes, la délivrance ciblée de médicaments ou encore la surveillance en temps réel de fonctions vitales. Si les défis techniques et éthiques restent nombreux, la précision de cette approche suscite déjà l’intérêt de la communauté scientifique.
| Points forts |
|---|
| La technique DISP (Deep Tissue In Vivo Sound Printing) utilise des ultrasons pour imprimer des polymères directement dans les tissus profonds du corps, marquant une rupture avec les méthodes conventionnelles limitées aux surfaces externes. De la chimiothérapie ciblée à la réparation tissulaire en passant par la surveillance cardiaque en temps réel, cette méthode ouvre des perspectives inédites en médecine régénérative. Le recours à des liposomes thermosensibles activés par une élévation localisée de 5°C garantit une polymérisation contrôlée, minimisant les risques pour les tissus environnants. |
Un tournant technologique : imprimer sous la peau sans incision
L’impression 3D médicale n’est plus une nouveauté, mais ses applications restent souvent limitées aux surfaces externes du corps ou à des greffes conçues préalablement en laboratoire. La méthode DISP change la donne en ciblant des tissus situés à plusieurs centimètres sous la peau. Contrairement aux techniques existantes basées sur la lumière infrarouge, dont la pénétration est restreinte aux couches superficielles, les ultrasons utilisés ici traversent les tissus épais avec une résolution millimétrique.
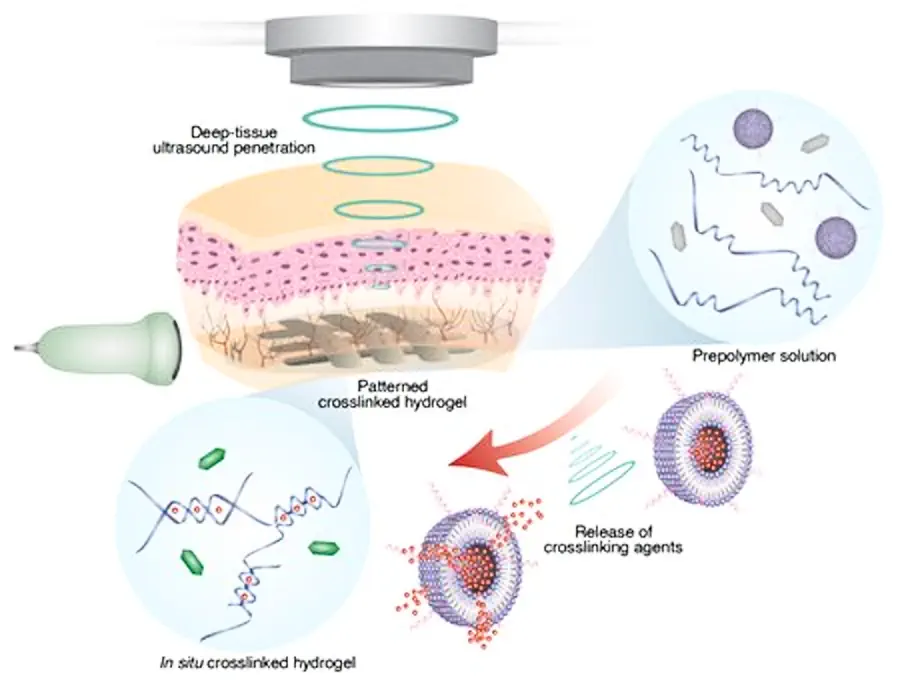
« Notre approche repose sur un contrôle localisé de la température », explique Wei Gao, professeur d’ingénierie médicale à Caltech et co-auteur de l’étude. Les chercheurs injectent d’abord une solution de bio-encre liquide, composée de monomères polymériques et de liposomes thermosensibles. Ces vésicules sphériques, activées par une élévation de 5°C induite par des ultrasons focalisés, libèrent un agent de réticulation qui déclenche la solidification du matériau. Le tout se produit en quelques secondes, sans altérer les cellules environnantes.
Pour visualiser le processus, l’équipe a intégré des vésicules gazeuses dérivées de bactéries (VGDB) dans la bio-encre. Ces structures protéiques, capables de refléter les ondes ultrasonores, agissent comme des marqueurs contrastants. « Elles nous permettent de suivre en temps réel la formation du réseau polymérique et d’ajuster les paramètres en fonction des besoins », précise Elham Davoodi, premier auteur de l’étude. Cette imagerie dynamique constitue un atout majeur pour garantir la fiabilité du dépôt.
Des applications variées, de la chimiothérapie aux capteurs internes
Les premiers tests, menés sur des souris, ont démontré l’efficacité de DISP dans deux domaines clés. Dans un premier cas, des polymères chargés de doxorubicine – un médicament anticancéreux – ont été imprimés près de tumeurs vésicales. Les résultats montrent une destruction cellulaire significativement supérieure à celle obtenue par injection classique, suggérant une concentration plus élevée du principe actif au site ciblé.
En second lieu, la technique a permis de sceller des lésions internes grâce à des gels bioadhésifs. Ces matériaux, conçus pour favoriser la cicatrisation, pourraient remplacer les sutures chirurgicales dans certains cas, réduisant ainsi les risques d’infection et le temps de récupération.
Mais l’un des aspects les plus innovants de DISP réside dans sa capacité à imprimer des hydrogels bioélectriques. Ces polymères conducteurs, intégrant des nanotubes de carbone ou des particules d’argent, pourraient servir de capteurs permanents pour surveiller des signaux physiologiques comme l’activité cardiaque. « Imaginez un dispositif intégré au cœur, capable de transmettre des données en continu sans nécessiter de chirurgie répétée », souligne Mikhail G. Shapiro, biologiste à Caltech.
Un défi multidisciplinaire : de la physique aux questions éthiques
Derrière cette percée se cache une collaboration entre experts en ingénierie, en biologie cellulaire et en acoustique. Financée par les National Institutes of Health, l’American Cancer Society et d’autres institutions, l’étude illustre l’importance croissante des approches interdisciplinaires en médecine.
Cependant, plusieurs verrous techniques doivent être levés avant toute application clinique. La biocompatibilité des matériaux reste un enjeu central : comment s’assurer qu’un polymère imprimé dans un organe ne provoquera pas de réactions inflammatoires à long terme ? Les chercheurs travaillent également à améliorer la résolution spatiale de DISP, notamment pour des interventions près de tissus délicats comme le système nerveux.
Newsletter Enerzine
Recevez les meilleurs articles
Énergie, environnement, innovation, science : l’essentiel directement dans votre boîte mail.
Autre défi : le développement de dispositifs externes capables d’interpréter les signaux émis par les hydrogels conducteurs. « Nous devons créer des interfaces capables de traiter ces données en temps réel, avec une précision clinique », ajoute Elham Davoodi. L’intégration d’algorithmes d’apprentissage automatique pourrait, à terme, permettre d’ajuster les paramètres d’impression en fonction des mouvements organiques, comme les battements cardiaques.
Enfin, les questions éthiques ne sont pas en reste. Comment encadrer l’usage de cette technologie pour éviter les dérives ? Quels critères définiront l’équité d’accès à ces traitements innovants ? « Il est crucial d’impliquer dès maintenant les comités d’éthique, les patients et les décideurs politiques », insiste Wei Gao.
Entre espoirs et prudence : un futur en construction
Malgré ces obstacles, DISP incarne un changement de paradigme. Pour la première fois, une méthode permet non seulement de réparer des tissus, mais aussi de créer des structures fonctionnelles in situ, adaptées aux besoins spécifiques de chaque individu. Cette flexibilité ouvre la voie à des thérapies personnalisées, où la précision l’emporterait sur les approches standardisées.
Cependant, les chercheurs restent mesurés. « Nous en sommes aux balbutiements », reconnaît Mikhail G. Shapiro. Les essais sur des modèles animaux plus proches de l’humain, suivis d’études cliniques, prendront probablement plusieurs années. En parallèle, le développement de normes régissant l’utilisation des ultrasons à haute intensité et des matériaux synthétiques dans le corps humain nécessitera un dialogue étroit entre scientifiques, régulateurs et société civile.
L’histoire de la médecine regorge d’inventions qui semblaient futuristes avant de devenir quotidiennes. L’impression 3D in vivo, portée par la DISP, pourrait bien suivre ce chemin. Mais son succès ne résidera pas seulement dans ses performances techniques : il dépendra aussi de sa capacité à s’intégrer dans un cadre éthique solide, garantissant que le progrès serve avant tout la santé des patients.
Lexique
- DISP (Deep Tissue In Vivo Sound Printing) : Méthode d’impression 3D médicale utilisant des ultrasons pour polymériser des matériaux directement dans les tissus vivants.
- Ultrasons focalisés : Ondes acoustiques concentrées sur une zone spécifique pour activer des réactions chimiques ou physiques avec une précision millimétrique.
- Liposomes thermosensibles : Vésicules sphériques encapsulant des agents de réticulation, libérant leur contenu lors d’une élévation localisée de température (environ +5°C).
- Bio-encre : Solution liquide composée de monomères polymériques, d’agents thérapeutiques (ex. : médicaments) et de marqueurs contrastants (ex. : VGDB), utilisée pour l’impression 3D in vivo.
- Vésicules gazeuses dérivées de bactéries (VGDB) : Structures protéiques remplies de gaz, reflétant les ultrasons et servant d’agents de contraste pour visualiser la polymérisation en temps réel.
- Hydrogels bioélectriques : Polymères conducteurs intégrant des nanotubes de carbone ou de l’argent, capables de surveiller des signaux physiologiques comme l’activité cardiaque.
- Biocompatibilité : Capacité d’un matériau à interagir avec les tissus vivants sans provoquer de réactions inflammatoires ou de rejet.
- Chimiothérapie ciblée : Administration précise de médicaments anticancéreux directement sur une tumeur, réduisant les effets secondaires systémiques.
- Imagerie ultrasonore en temps réel : Technique permettant de visualiser et d’ajuster les processus d’impression in vivo grâce à des marqueurs contrastants comme les VGDB.
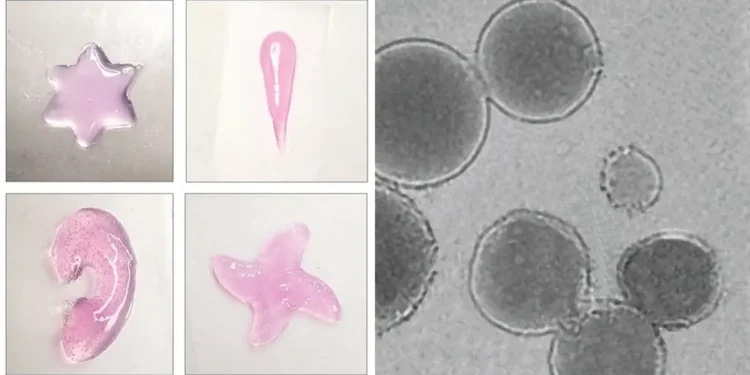
Légende illustration : (G) Quelques structures de polymères hydrogel imprimées avec la technique d’impression sonore in vivo. (D) Image TEM des liposomes sensibles à basse température de l’équipe, chargés d’un agent de réticulation. Crédit : Elham Davoodi et Wei Gao
Article : « Imaging-guided deep tissue in vivo sound printing » – DOI : 10.1126/science.adt0293